Saúde
Anvisa autoriza estudo clínico de vacina Sanofi Pasteur no Brasil
O estudo prevê a aplicação de duas doses, e a Bahia está entre os estados onde serão feitos os testes.
Publicado
em
Por
Daniela Oliveira
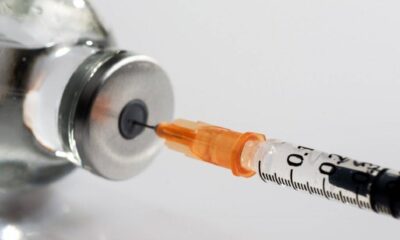
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a realização de estudos clínicos da vacina contra a Covid-19 da farmacêutica francesa Sanofi Pasteur, no Brasil.
Segundo a Anvisa, o estudo clínico inicial será dividido em duas fases e deve envolver 150 voluntários com 18 anos ou mais de idade. O objetivo do estudo é testar três diferentes dosagens da vacina, para definir a dose ideal antes de prosseguir para um estudo de fase III.
O estudo prevê a aplicação de duas doses, com 21 dias de intervalo. Participarão voluntários de quatro estados: Bahia, Minas Gerais, Mato Grosso do Sul e Rio de Janeiro. Ainda de acordo com a Anvisa, o início do estudo depende apenas da apresentação dos resultados dos estudos de estabilidade da vacina, que definem o prazo de validade do produto.
Este é o nono estudo de vacina contra a Covid-19 autorizado pela Anvisa no Brasil.
Leia Também
-
SMS amplia vacinação contra a dengue para público de 6 a 16 anos
-


Ministério da Saúde amplia público-alvo de vacinação contra a dengue com doses próximas do vencimento
-


Vacina para cães contra dez doenças é disponibilizada no Parque da Cidade nesta quinta e sexta
-


Doação de sangue e vacinação movimentam Parque Shopping Bahia neste sábado em Lauro de Freitas
-
Prefeitura convoca pré-adolescentes para se vacinarem contra a dengue
-
Salvador conta com mais de 50 pontos de vacinação contra gripe e dengue neste sábado

Com atuação em Camaçari, O Boticário abre vaga na área de automação e digitalização; veja requisitos

Flávio acusa estado de suspender convênio com prefeitura e não pagar R$ 11 milhões ao município

Simm tem 45 vagas de emprego para Salvador e Simões Filho nesta sexta; confira lista

Eleições: Oswaldinho não descarta possibilidade de montar chapa ‘puro-sangue’

Evento de MMA acontece no Parque Shopping Bahia neste fim de semana

Polícia Civil prende quatro suspeitos de sequestro de médico em Salvador

Projeto-piloto da feira livre do bairro Santo Antônio terá apoio do grupo ‘Mulheres das Enxadas’

‘Show da Cufa’ reúne Solange Almeida, Tayrone, Ana Catarina e Thiago Aquino em Lauro de Freitas

CLN abre vaga exclusiva para pessoa com deficiência em Camaçari

Abril da Dança é marcado por oficinas artísticas gratuitas em Camaçari e segue até segunda

Eleições: Oswaldinho não descarta possibilidade de montar chapa ‘puro-sangue’

STT regulamenta táxis na cor branca para operarem no município

Horto Florestal recebe projeto Eco Dança nesta sexta

TCM aprova contas de 2022 da Secretaria de Saúde de Camaçari na gestão de Elias Natan

Em alerta laranja, Camaçari terá chuvas intensas até sábado

Flávio acusa estado de suspender convênio com prefeitura e não pagar R$ 11 milhões ao município

Evento de MMA acontece no Parque Shopping Bahia neste fim de semana

Segunda audiência pública sobre revisão da Lei Orgânica Municipal será em Vila de Abrantes

Dia D de vacinação contra a gripe acontece no Shopping Bela Vista neste sábado

Arraiá do Horto: ingressos para segunda edição já estão disponíveis

Caixa paga parcela de abril do Bolsa Família a beneficiários com NIS de final 8

Simm tem 45 vagas de emprego para Salvador e Simões Filho nesta sexta; confira lista

Inscrições para o concurso Kit Cultura Popular terminam nesta sexta

Com atuação em Camaçari, O Boticário abre vaga na área de automação e digitalização; veja requisitos

O novo já nasceu velho, por Jaqueline Andrade

1xBet se torna parceira oficial da Associação Carlos Barbosa de Futsal










