Saúde
AstraZeneca testará nova versão de vacina e terceira dose na Bahia
O teste também será feito em outros estados brasileiros, no Reino Unido, África do Sul e Polônia.
Publicado
em
Por
Agência Brasil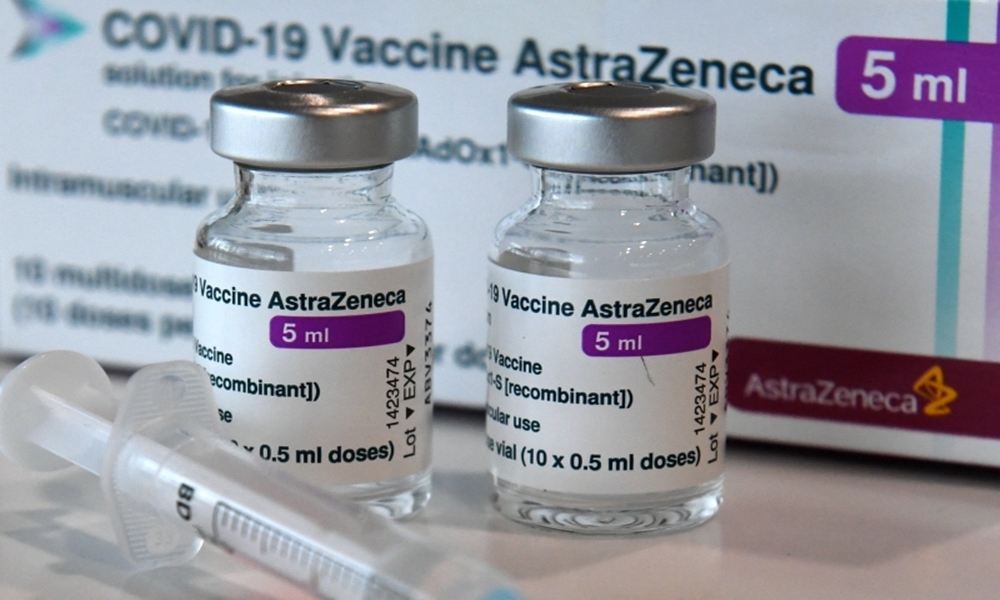
A Bahia está entre os cinco estados que sediarão pesquisa clínica aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa), para testagem da vacina (AZD2816) desenvolvida pela AstraZeneca.
O imunizante será fabricado pela empresa Symbiosis Pharmaceutical Services, sediada no Reino Unido, e é uma nova versão da vacina já aplicada no Brasil (AZD1222). Ela foi modificada para também fornecer imunidade contra a recém-emergente cepa da variante B.1.351 da Covid-19, identificada primeiro na África do Sul, em abril.
O estudo, de fase II/III parcialmente duplo-cego, randomizado, será aplicado em adultos de 18 anos de idade ou mais, previamente vacinados e não vacinados para determinar a segurança e a imunogenicidade da vacina candidata.
A AstraZeneca quer verificar a eficácia do imunizante, que atuaria como uma espécie de terceira dose para indivíduos soronegativos para SARS-CoV-2, que receberam anteriormente uma vacinação primária de duas doses contra a covid-19 SARS-CoV-2 com a vacina atualmente em uso (AZD1222) ou de uma vacina que utiliza a tecnologia de RNA mensageiro (mRNA) contra a covid-19, como as da Pfizer e da Moderna.
Também será verificada a eficácia da candidata a imunizante sendo aplicada como vacinação homóloga primária de duas doses para pessoas soronegativas para SARS-CoV-2 que não estão vacinadas”.
Nesse caso, os pesquisadores querem testar uma espécie de esquema misto, com a aplicação de uma primeira dose da vacina da AstraZeneca já utilizada no país e a segunda dose da nova versão do produto.
A empresa planeja testar esse esquema em 2.475 participantes no Brasil, Reino Unido, África do Sul e Polônia. No Brasil está prevista a participação de 800 pessoas, além da Bahia, no Distrito Federal, Paraná, Rio Grande do Norte, Rio Grande do Sul e São Paulo.
Leia Também
-


São João na Bahia: Governo lança editais para seleção e contratação de grupos
-


Três policiais investigados por participação em grupo de extermínio são presos na Bahia
-


Com alerta laranja de chuvas intensas, Defesa Civil alerta para cuidados com a leptospirose
-


Polícia Militar intensifica ações em 417 municípios baianos durante Operação Força Total
-


CCR Metrô amplia horário de funcionamento para jogo do Bahia e Fluminense nesta terça
-


Inscrições do Programa Partiu Estágio encerram na próxima sexta

Senai abre processo seletivo para vaga de almoxarife em Camaçari

Saiba como será o funcionamento do Boulevard Shopping no feriado de Tiradentes

Continental abre processo seletivo para Jovem Aprendiz em Camaçari; veja como se inscrever

“Dar uma casa para minha mãe”, afirma Davi após ganhar o BBB24

Motorista por aplicativo sofre tentativa de latrocínio após aceitar corrida para Camaçari

Em São Paulo, Flávio Matos participa de feira internacional de turismo

SineBahia: veja vagas em Salvador, Simões Filho, Lauro de Freitas e Camaçari

Rose Braga apresenta prato com ingredientes produzidos em Camaçari no programa Mais Você

Condenado a 17 anos de prisão por estupro de vulnerável é preso em Lauro de Freitas

Congresso sobre direito das famílias e sucessões terá painéis e mesas-redondas em Salvador

São João na Bahia: Governo lança editais para seleção e contratação de grupos

Prefeitura convoca candidatos para prova de títulos do cargo de procurador

Teatro Gamboa recebe show ‘Daniel Bispo canta Lado B Djavan’ neste fim de semana

Com programação gratuita, Festa Literária Internacional da Praia do Forte ocorre em maio

Três policiais investigados por participação em grupo de extermínio são presos na Bahia

Embasa divulga lista de 35 candidatos aprovados no concurso público

Primeira quinzena de abril tem maior volume de chuva dos últimos 30 anos em Salvador

Consulta pública eletrônica sobre elaboração do PL-LDO 2025 encerra sexta

Motorista por aplicativo sofre tentativa de latrocínio após aceitar corrida para Camaçari

Continental abre processo seletivo para Jovem Aprendiz em Camaçari; veja como se inscrever

“Dar uma casa para minha mãe”, afirma Davi após ganhar o BBB24

Projetos de professores de Lauro de Freitas são premiados em São Paulo e escolas recebem R$ 30 mil

Com alerta laranja de chuvas intensas, Defesa Civil alerta para cuidados com a leptospirose

Atualização da Lei Orgânica de Camaçari será pautada em audiência pública nesta quinta

Senai abre processo seletivo para vaga de almoxarife em Camaçari

Plano Inclinado Gonçalves funciona em horário ampliado








