Geral
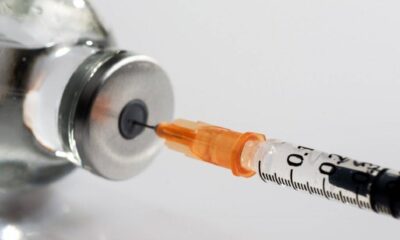
Anvisa retira obrigação de testes no Brasil para autorização de vacinas
Medida vai facilitar registro de novos imunizantes no país.
Publicado
em
Por
Agência BrasilA Agência Nacional de Vigilância Sanitária (Anvisa) anunciou nesta quarta-feira (3) o fim da exigência de estudos da fase três, em andamento no Brasil para autorização emergencial de vacinas no país. Essa é a principal mudança trazida na atualização do guia para uso emergencial de imunizantes contra a Covid-19. São os estudos da fase três que mostram o percentual de eficácia da vacina, quantas doses devem ser aplicadas, além da avaliação de eventuais reações adversas. 

“Essa atualização faz parte da estratégia regulatória do Brasil de favorecer acesso. Ela está apartada de qualquer discussão que seja fora do âmbito técnico, para que o Brasil garanta que tenha acesso a vacinas com qualidade, eficácia e segurança”, disse a diretora da Anvisa, Meiruze Freitas, durante coletiva de imprensa para comunicar as alterações.
Com a mudança, a norma da Anvisa segue exigindo estudo de desenvolvimento clínico da vacina na fase 3, mas agora ele não precisa estar sendo conduzido no Brasil. O guia passa a contar com a seguinte redação: “A vacina deve preferencialmente possuir um Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) anuído pela Anvisa e o ensaio clínico fase 3, pelo menos, em andamento e em condução no Brasil”. No caso de fase três realizada no exterior, caberá ao laboratório requerente apresentar os dados brutos do estudo, fazer o acompanhamento dos participantes dos testes para avaliação de eficácia por pelo menos um ano, e apresentar demonstração de que os estudos pré-clínicos e clínicos foram conduzidos conforme as diretrizes aceitas nacional e internacionalmente. O prazo de análise para vacinas sem estudo de fase três desenvolvido no Brasil será de até 30 dias.
“A vacina com estudo de fase três aqui no Brasil ou no exterior vai ter que seguir o mesmo critério de segurança, qualidade e eficácia. A única diferença vai ser a necessidade de apresentar dados que permitam que nós tenhamos confiança no estudo no exterior e que esse estudo mostre que a vacina serve para a população brasileira. E nós, como agência reguladora, vamos assegurar isso”, afirmou Gustavo Mendes, gerente-geral de medicamentos da Anvisa.
Até agora, no Brasil, existem duas vacinas com autorização de uso emergencial: a CoronaVac, desenvolvida pelo Instituto Butantan em parceria com a Sinovac, e o imunizante desenvolvido pela farmacêutica AstraZeneca, em parceria com a Fundação Oswaldo Cruz (Fiocruz). A flexibilização nas regras do pedido de uso emergencial pode beneficiar, por exemplo, o laboratório União Química, que está à frente da produção da vacina russa Sputnik V no Brasil. O imunizante ainda aguarda autorização de estudo fase três no país, mas agora não dependerá mais desse pré-requisito para encaminhar o pedido.
De acordo com Meiruze Freitas, a expectativa é que a nova redação do guia para uso emergencial amplie a oferta de vacinas no país. “A gente ainda não recebeu isso diretamente de nenhuma empresa, mas eu espero fortemente que tenha impacto. Isso certamente possibilitaria para a Moderna, Novavax e um monte de outras vacinas, dentro inclusive do portfólio da Covax Facility “.
Leia Também
-


Local de prova do Concurso Nacional Unificado é disponibilizado nesta quinta
-


Beneficiários do INSS começam a receber o 13º a partir desta quarta-feira
-


Cássia Valle lança coleção sobre heroínas negras brasileiras na Bienal do Livro da Bahia
-
SMS amplia vacinação contra a dengue para público de 6 a 16 anos
-


Após 18 anos, primeiro caso de cólera autóctone é registrado no Brasil; paciente é de Salvador
-


‘Cometa do Diabo’ ficará visível no Brasil neste domingo; veja horário

“Eu não resolvo só abrindo hospitais”, dispara Jerônimo sobre críticas à regulação e ao HGC

Dia Internacional da Dança é comemorado no Shopping Paseo nesta quinta

Elinaldo x Caetano: 2 a 0 é o placar
Produtora baiana convoca atores e atrizes para elenco de série gravada em Salvador

Manuel Rocha solicita que HGC volte a atender por demanda espontânea

Mega-Sena sorteia prêmio estimado em R$ 6 milhões nesta quinta

Pedido de isenção da taxa de inscrição para o Enem pode ser feito até sexta

“Nossa ideia é passar os próximos anos instalados aqui”, afirma vice-presidente da Goldwind em visita a Camaçari

USF Camaçari de Dentro oferece serviços de saúde para homens e mulheres neste sábado

Confira as 68 vagas de emprego do Simm para Salvador; veja lista e requisitos

Local de prova do Concurso Nacional Unificado é disponibilizado nesta quinta

Bolsa Família: Caixa paga parcela de abril a beneficiários com NIS de final 7

SineBahia divulga vagas para Salvador, Lauro de Freitas, Camaçari e Dias d’Ávila

“O nosso Polo está pronto para receber novas indústrias”, garante Ivoneide Caetano

Na China, presidente do Sindborracha firma protocolo de irmandade com sindicatos de Henan

“Eu não resolvo só abrindo hospitais”, dispara Jerônimo sobre críticas à regulação e ao HGC

Elinaldo x Caetano: 2 a 0 é o placar

Teatro Vila Velha apresenta espetáculo ‘AGNI’ em Salvador neste domingo

Manuel Rocha solicita que HGC volte a atender por demanda espontânea

Requalificação das vias do Polo Industrial de Camaçari terá início no próximo dia 2, afirma governador
Produtora baiana convoca atores e atrizes para elenco de série gravada em Salvador

Dia Internacional da Dança é comemorado no Shopping Paseo nesta quinta

Caixa paga Bolsa Família e Auxílio-Gás a beneficiários com NIS de final 6

Velório da ex-vereadora Margarida Galvão ocorre no Barracão Comunitário de Arembepe

Duas mulheres são presas em flagrante por tráfico de drogas em Camaçari

Homem tem mandado cumprido por tentativa de feminicídio em Mata de São João









