Destaque
Anvisa quer mais dados para autorizar uso de vacina produzida na Índia
Pedido foi feito em reunião com representantes da Fiocruz.
Publicado
em
Por
Agência Brasil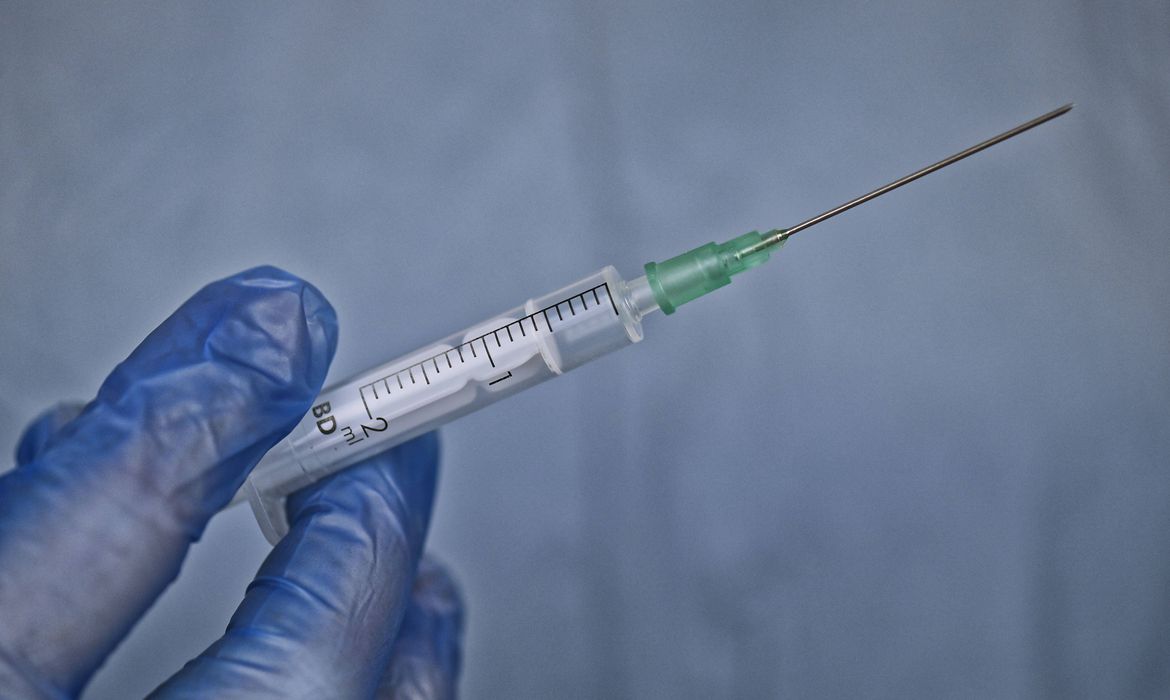
Em nova reunião com representantes da Fundação Oswaldo Cruz (Fiocruz), a Agência Nacional de Vigilância Sanitária (Anvisa) reforçou ontem (4) o pedido de mais informações para liberar a autorização emergencial do uso das doses da vacina contra a Covid-19 que serão importadas do Serum Institute of India, que produz o imunizante da Oxford e AstraZeneca na Índia, onde o uso emergencial já foi aprovado.

No dia 31 de dezembro de 2020, a Anvisa autorizou a importação, em caráter excepcional, de 2 milhões de doses da vacina britânica da Oxford, produzida em parceria com a Fiocruz no Brasil. As doses importadas foram fabricadas. Em nota, a agência reguladora informa que fez, na manhã desta segunda-feira, uma reunião para tratar da submissão do protocolo do uso emergencial das doses da vacina.
Na reunião, representantes da Fiocruz apresentaram os dados já de posse da fundação, e a agência reguladora listou informações, ainda aguardadas pela Fiocruz, necessárias para o pedido de autorização para uso emergencial da vacina no Brasil.
“Na reunião, a Fiocruz mostrou que está empenhada para que essas informações sejam reunidas e apresentadas à Anvisa com a maior brevidade”, diz a nota.
A Anvisa quer saber se o produto do fabricante indiano é semelhante ao fabricado no Reino Unido, que teve os dados clínicos aprovados, e se o método de produção e os materiais utilizados são os mesmos. “Para a autorização, a agência precisa avaliar os estudos de comparabilidade entre a vacina do estudo clínico, que é fabricada no Reino Unido, com a vacina fabricada na Índia, bem como os dados de qualidade e condições de boas práticas de fabricação e controle”, acrescenta o texto.
Segundo a Anvisa, as informações servirão para avaliar a equivalência da vacina produzida na Índia quanto à resposta da imunogenicidade. O termo diz respeito à habilidade da vacina de ativar resposta ou reação imune contra o coronavírus, tais como o desenvolvimento de anticorpos específicos, respostas de células T, reações alérgicas ou anafiláticas. “Ou seja, é necessário entender se o produto do fabricante indiano é semelhante ao fabricado no Reino Unido e que teve os dados clínicos aprovados”, reforça a Anvisa.
A agência diz ainda que não fará nenhum retrabalho durante sua análise e que já tem trabalhado para aproveitar a análise de agências de referência e focar em questões que são específicas para o Brasil. “A Anvisa e a Fiocruz seguem em comunicação para otimizar as avaliações e a entrega dos documentos necessários para avaliação e decisão da agência”, informa a Anvisa.
Leia Também
-


USF Camaçari de Dentro oferece serviços de saúde para homens e mulheres neste sábado
-
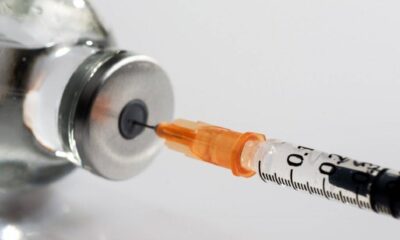
SMS amplia vacinação contra a dengue para público de 6 a 16 anos
-


Espaço Cidadania oferece serviços gratuitos durante a semana em Salvador; confira a programação
-


Maio Roxo: campanha chama atenção para doenças inflamatórias intestinais
-


Ministério da Saúde amplia público-alvo de vacinação contra a dengue com doses próximas do vencimento
-
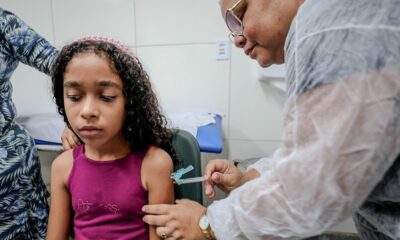
Sesau amplia vacinação contra dengue para novo público em Camaçari

“Eu não resolvo só abrindo hospitais”, dispara Jerônimo sobre críticas à regulação e ao HGC
Produtora baiana convoca atores e atrizes para elenco de série gravada em Salvador

Elinaldo x Caetano: 2 a 0 é o placar

Requalificação das vias do Polo Industrial de Camaçari terá início no próximo dia 2, afirma governador

Manuel Rocha solicita que HGC volte a atender por demanda espontânea

Marcos Semeadores, Nara Costa e Nengo Vieira estão entre atrações do Abala Abrantes

“Ele não dá boa notícia, é só ‘oba oba’ para fazer politicagem”, dispara Flávio Matos sobre Caetano

Lauro de Freitas passa integrar ações do programa Corra pro Abraço

Centro Universitário oferece curso gratuito de atendente de farmácia em Salvador

Setor turístico de Camaçari tem potencial de geração de emprego maior que o Polo, destaca Bacelar

Boulevard Shopping Camaçari sediará primeiro ‘Encontro de Carros Antigos’ em maio

Sindborracha comemora Dia do Trabalhador com shows de Simpa e Edy Xote

Polícia apreende drogas sintéticas em encomendas dos Correios em Simões Filho e Salvador

Mega-Sena sorteia prêmio estimado em R$ 6 milhões nesta quinta

Pedido de isenção da taxa de inscrição para o Enem pode ser feito até sexta

“Nossa ideia é passar os próximos anos instalados aqui”, afirma vice-presidente da Goldwind em visita a Camaçari

USF Camaçari de Dentro oferece serviços de saúde para homens e mulheres neste sábado

Confira as 68 vagas de emprego do Simm para Salvador; veja lista e requisitos

Local de prova do Concurso Nacional Unificado é disponibilizado nesta quinta

Bolsa Família: Caixa paga parcela de abril a beneficiários com NIS de final 7

SineBahia divulga vagas para Salvador, Lauro de Freitas, Camaçari e Dias d’Ávila

“O nosso Polo está pronto para receber novas indústrias”, garante Ivoneide Caetano

Na China, presidente do Sindborracha firma protocolo de irmandade com sindicatos de Henan

“Eu não resolvo só abrindo hospitais”, dispara Jerônimo sobre críticas à regulação e ao HGC

Elinaldo x Caetano: 2 a 0 é o placar

Teatro Vila Velha apresenta espetáculo ‘AGNI’ em Salvador neste domingo









